Los implantes brindan muchos beneficios, tanto físicos como psicológicos, ya sea que una mujer los elija por razones estéticas o para la reconstrucción mamaria después de una cirugía de cáncer. Pero también traen riesgos.
“Una mujer que decide tener implantes mamarios debe saber que es posible que no duren para siempre”, dice la Dra. Andrea Pusic, profesora de cirugía Joseph E. Murray en la Escuela de Medicina de Harvard.
“Eso significa que es posible que necesite una cirugía en el futuro o que tenga complicaciones a largo plazo.
La cirugía es una decisión seria y los dispositivos no son perfectos”.
La FDA se movió recientemente para ayudar a asegurarse de que las mujeres que consideran los implantes mamarios tengan una idea clara de lo que implican los implantes antes de continuar con la cirugía. La agencia anunció una serie de cambios en octubre de 2021, incluidos estos:
*Establecer nuevos requisitos de etiquetado para los fabricantes de implantes mamarios, incluido un recuadro de advertencia.
*Permitir la venta de implantes mamarios solo a establecimientos que acepten proporcionar a los pacientes una lista de verificación completa que describa los riesgos y beneficios potenciales relacionados con los implantes mamarios
*Actualizar las recomendaciones de detección diseñadas para detectar fugas en los implantes mamarios de silicona
*Publicar información actualizada sobre estudios posteriores a la aprobación de implantes mamarios para informar mejor a los pacientes.
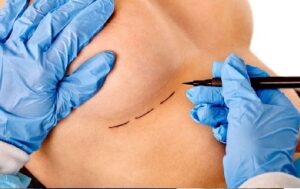 Los cambios son buenas noticias para las mujeres, dice la Dra. Pusic.
Los cambios son buenas noticias para las mujeres, dice la Dra. Pusic.
“La cirugía de implantes mamarios nunca ha sido más segura, porque la tecnología de los implantes ha mejorado y las tasas de fugas son más bajas que nunca.
Además, las complicaciones quirúrgicas también son más bajas, gracias a las nuevas técnicas y estrategias.
Ahora, las mujeres obtienen una seguridad adicional de que la FDA también participa activamente en garantizar que los implantes mamarios sean seguros y que todas las mujeres estén bien informadas”, dice.
Los cambios de la FDA fueron impulsados por un panel de cirujanos, científicos, mujeres y grupos de defensa reunidos en la primavera de 2019.
Inmediatamente después de la reunión, la FDA tomó medidas para prohibir la venta de implantes mamarios texturizados, que estaban relacionados con un riesgo elevado de un cáncer raro llamado linfoma anaplásico de células grandes.
A las mujeres con los implantes no se les aconsejó que se los quitaran, pero se les dijo que estuvieran atentas a los cambios en los senos.
Otra lección aprendida de la reunión fue que algunas mujeres que han optado por ponerse implantes pueden haberlo hecho sin comprender claramente todos los inconvenientes potenciales asociados con el procedimiento.
Uno de los riesgos en los que se centró el panel es la enfermedad de los implantes mamarios, una serie de síntomas que incluyen fatiga, ansiedad y depresión, dolor en el pecho y pérdida de cabello que algunas mujeres creen que están relacionados con sus implantes.
“No hay duda de que una minoría de mujeres con implantes mamarios reportan síntomas.
Todavía no está claro si estos síntomas son causados por los implantes mamarios o si son causados completamente por otra cosa”, dice el Dr. Pusic.
Pero los investigadores están tratando de averiguarlo.
Mientras tanto, la FDA quiere que las mujeres que estén considerando someterse a una cirugía de implante sepan que algunas mujeres experimentan estos síntomas después del procedimiento.
La nueva lista de verificación ayuda a informar a las mujeres sobre este y otros riesgos potenciales, como complicaciones quirúrgicas y ruptura de implantes mamarios.
“Lo más importante es que podemos hacerlo mejor en términos de informar a los pacientes sobre los riesgos y beneficios de los implantes mamarios”, dice el Dr. Pusic.
Monitoreo de problemas
Además de exigir la lista de verificación, la FDA cambió sus recomendaciones para evaluar a las mujeres con implantes de silicona en busca de fugas en un esfuerzo por alentar a más mujeres a hacerse la revisión.
“Los implantes de silicona se reintrodujeron en los Estados Unidos en 2006”, dice el Dr. Pusic.
Habían sido retirados del mercado después de que surgieron problemas relacionados con las fugas de los implantes mamarios y que permitían que la silicona se filtrara en el cuerpo.
Para identificar y tratar rápidamente este problema antes de que se convierta en un riesgo para la salud, la FDA recomienda que las mujeres con implantes de silicona se sometan a pruebas de detección de fugas cada dos años.
Los funcionarios inicialmente recomendaron que esto se hiciera usando MRI.
Si bien esta estrategia fue ciertamente efectiva para identificar la ruptura del implante mamario, muchas mujeres no siguieron la recomendación.
 No solo era costoso, hasta $2,000 de su bolsillo por cada resonancia magnética, sino que para algunas mujeres, las resonancias magnéticas también eran una fuente de ansiedad, dice el Dr. Pusic.
No solo era costoso, hasta $2,000 de su bolsillo por cada resonancia magnética, sino que para algunas mujeres, las resonancias magnéticas también eran una fuente de ansiedad, dice el Dr. Pusic.
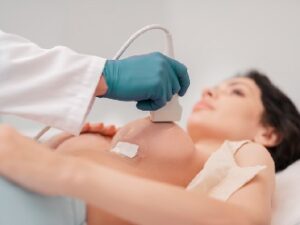
La FDA ahora recomienda una alternativa más fácil y económica: los exámenes de ultrasonido.
El ultrasonido se puede usar para la vigilancia de rutina y los problemas potenciales, confirmados mediante resonancia magnética.
Estas nuevas medidas deberían garantizar que las mujeres estén informadas e inspirar confianza en quienes consideran los implantes.
Los implantes mamarios pueden brindar beneficios a la paciente adecuada, una que esté bien informada sobre los pros y los contras del procedimiento.
Pero las mujeres deben tener claro que el procedimiento sigue siendo una cirugía y que los implantes mamarios son dispositivos médicos y deben ser considerados como tales, dice.




